Подбор доноров для трансплантации фекальной микробиоты: невольный скрининг здоровья населения
На сегодняшний день многие заболевания связаны с микробиотой кишечника, включая инфекционные состояния (инфекционный гастроэнтерит, клостридиальная инфекция), аутоиммунные заболевания [аллергические заболевания, диабет, воспалительные заболевания кишечника (ВЗК)], некоторые общие состояния (избыточный вес, функциональные расстройства ЖКТ). Восстановление нормальной микробиоты кишечника в последние годы стало предметом многих фундаментальных и клинических исследований.
Обнаруженная связь между микробиотой и заболеваниями у людей – предмет значительного клинического интереса. Использование трансплантации фекальной микробиоты (ТФМ) для лечения многих заболеваний приводит к значительным долгосрочным изменениям кишечной микробиоты со сдвигом в сторону состава донорской микробиоты и представляет собой относительно безопасную процедуру для пациентов без долгосрочных побочных эффектов [1].
ТФМ стала высокоэффективным методом лечения (бактериотерапией) при рецидивирующей инфекции Clostridioides difficile. С 2013 г. ТФМ официально одобрена Управлением по контролю пищевых продуктов и лекарственных препаратов США (Food & Drug Administration) для терапии и предупреждения рецидивов кишечной инфекции, вызванной ванкомицин-устойчивой формой бактерии Clostridioides difficile [2–4]. В 2022 г. FDA впервые зарегистрирован препарат фекальной микробиоты Rebyota (https://www.rebyota.com/) (ректальное введение), а в мае 2023 г. был одобрен пероральный препарат Vowst (https://www.vowsthcp.com/).
Отмечена эффективность ТФМ для лечения других острых и хронических заболеваний, связанных с микробным дисбиозом. Определение эффективности в первую очередь основано на положительном клиническом ответе у реципиента [5]. Однако с микробиологической точки зрения успех ТФМ также может определяться изменением профиля микробиома кишечника реципиента в сторону профиля микробиома донора [2].
Успешность метода использования ТФМ при лечении заболеваний, связанных с изменением нормальной микробиоты кишечника, неразрывно связана с необходимостью проведения всестороннего строгого скрининга населения для отбора потенциальных доноров [6].
Процедура ТФМ состоит из трех основных этапов: поиск и обследование донора, подготовка фекального материала и введение его пациенту. Выбор и скрининг доноров является одним из наиболее важных аспектов ТФМ, так как он должен обеспечить ее безопасность для реципиента. Чаще всего отбор доноров включает анкетирование, физикальное обследование, а также лабораторный анализ состояния его здоровья и взятого у него материала фекалий [7–9].
При правильной организации скрининга методологические подходы в организации скрининговых программ населения по поиску доноров фекальной микробиоты должны быть едиными и эффективными; связаны с целями проводимого скрининга, однако они могут отличаться на уровне популяционных групп или географических регионов. Отбор здоровых добровольцев, которые могут стать донорами фекальной микробиоты, происходит в процессе скрининга, включающего несколько этапов [10].
В Российской Федерации термин «скрининг» употребляется как синоним первого этапа диспансеризации [11]. На этом этапе скрининга из общей популяции выделяются лица, относящиеся к первой группе здоровья по результатам диспансеризации, считающие себя здоровыми, у которых не было клинических признаков заболевания или факторов риска их развития, а при лабораторно-инструментальных исследованиях не выявлены изменения, выходящие за референтные значения. Однако в категорию здоровых добровольцев могут быть включены не все кандидаты из этой группы [12].
Следующий этап скрининга подразумевает отбор кандидатов, соответствующих критериям приемлемости включения в исследование. В соответствии с рекомендациями по надлежащей клинической практике исследователь несет ответственность за то, чтобы в исследование включались только подходящие субъекты. Приемлемость определяется на основе критериев включения и исключения в исследование. В настоящее время единых критериев, однозначно описывающих здорового добровольца, не существует. Тем не менее международным экспертным сообществом определены критерии исключения для кандидатов в доноры фекальной микробиоты [13].
К таковым относятся указания в анамнезе на факт заболевания некоторыми инфекционными болезнями (ВИЧ, вирусные гепатиты, сифилис, малярия, туберкулез, зоонозные инфекции), а также факторы риска передачи возбудителей инфекционных заболеваний от потенциального донора реципиенту (использование внутривенных наркотиков, рискованное сексуальное поведение, недавние трансфузии препаратов крови, манипуляции с потенциально нестерильным хирургическим инструментарием, татуировки, пирсинг, акупунктура, поездки в эпидемически неблагополучные районы, вакцинация живыми вакцинами), неинфекционные заболевания (синдром раздраженного кишечника, ВЗК, ожирение, психические и неврологические заболевания, аутоиммунные заболевания кишечника, следование строгим ограничительным диетам) и препараты (антибиотики, цитостатики, иммунодепрессанты, ингибиторы протонной помпы), способные изменять состав кишечной микробиоты.
Лабораторное обследование донора должно включать общий анализ крови с полным дифференцированным подсчетом клеток крови и обязательной «ручной» микроскопией мазка крови, исследование крови на цитомегаловирус, вирусы Эпштейна–Барр, гепатита (А, В, С, D, Е), сифилис, ВИЧ-1 и ВИЧ-2, Entamoeba histolytica, С-реактивный белок и скорость оседания эритроцитов, альбумин, креатинин и электролиты, аминотрансферазы, билирубин, γ-глутамилтрансферазу, щелочную фосфатазу; общее исследование кала, обнаружение в нем Clostridioides difficile, выявление кишечных возбудителей, в том числе сальмонелл, шигелл, Campylobacter, Escherichiacoli O157:H7, Yersinia spp., ванкомицин-резистентных энтерококков, метициллин-резистентного Staphylococcus aureus, грамотрицательных полирезистентных бактерий, норовирус, антигены и/или кислотоустойчивое окрашивание Giardia lamblia и Criptosporidium parvum, простейших (включая Blastocystis hominis) и гельминтов, анализ кала на скрытую кровь, антигены и/или кислотоустойчивое окрашивание на изоспоры и микроспоридии, кальпротектин, фекальный антиген Helicobacter pylori, ротавирусы [14].
Кроме того, при подборе донора для ТФМ могут быть учтены данные медико-генетического обследования донора и реципиента, качественные и количественных показатели иммунного статуса пациента [15].
При подборе донора ТФМ могут быть применены дополнительные программы стандартизации, как при выборе потенциального здорового донора (родственный, неродственный), так в процессе подготовки донорского материала (свежий или замороженный, аэробный или анаэробный) или дозы, метода введения (клизмы, капсулы, введение через назогастральный зонд, с помощью эндоскопа), частоты использования (однократно или с определенной частотой).
В качестве перспективного направления скрининга можно рассматривать персонализированные стратегии изучения таксономической структуры, определение видового разнообразия фекальной микробиоты донора и реципиента, их дальнейшее сопоставление с использованием технологий искусственного интеллекта [16].
У донора, не имеющего критериев исключения, в день донорства должно быть проведено дополнительное анкетирование, включающее исключение медицинских событий или факторов риска их развития [признаки желудочно-кишечного кровотечения, недавно возникшего инфекционного заболевания (тошнота, жидкий стул, першение в горле, увеличение лимфоузлов, желтуха и др.), использование антибиотиков или других препаратов, которые могут ухудшить микробиоту кишечника, новые половые партнеры или поездки за границу после проведенного скрининга].
За последнее столетие ускорение темпов научно-технического прогресса и урбанизация привели к кардинальному изменению образа жизни человека. Беспрецедентными темпами происходит изменение окружающей среды. Употребление в пищу преимущественно обработанных продуктов, приверженность определенному питанию, изменение взглядов на гигиенические мероприятия, использование антибиотиков при лечении инфекционных заболеваний привело к уничтожению некоторых бактерий и снижению разнообразия микробиоты кишечника.
В мире предприняты попытки сохранить разнообразие микробиоты кишечника. Так, учеными Швейцарии, США, Германии запущен проект по созданию хранилища микробиоты – банка замороженных образцов кала с различными микроорганизмами (https://www.microbiotavault.org/). Проект направлен на сохранение биоразнообразия микробиоты, пока это еще возможно, путем создания учреждения для безопасного хранения и консервации образцов и коллекций микробиоты. Рост числа успешных клинических исследований по ТФМ при различных заболеваниях способствовал открытию биобанка фекальной микробиоты в 2012 г. В настоящее время банк фекальной микробиоты предоставляет возможность постоянного доступа к образцам донорской фекальной микробиоты более чем 750 клиникам во всех штатах США. В России все вопросы с выбором донора фекальной микробиоты также могут быть решены путем создания соответствующих биобанков, которые будут заниматься поиском, обследованием, подбором доноров, а также хранением и доставкой фекальной микробиоты в медицинские организации.
Цели работы – подбор доноров фекальной микробиоты для ТФМ, непроизвольный скрининг здоровья населения, а также формирование предпосылок для создания биобанка образцов фекальной микробиоты здоровых доноров.
Материал и методы
Первичный подбор доноровВ исследование были включены 73 здоровых добровольца – потенциальных донора фекальной микробиоты, мужского и женского пола (рандомная выборка жителей г. Москвы и Мос- ковской области на основании личного желания стать донором). Первичный отбор доноров проводился на основании анкетирования и согласно ранее разработанному алгоритму: возраст от 18 до 55 лет; индекс массы тела (ИМТ) донора – 18,5–24,99 кг/м2; нормальный ежедневный стул в течение 3 нед; отсутствие в анамнезе ВЗК и онкологических заболеваний, хронических инфекционных, аутоиммунных, атопических заболеваний или каких-либо аллергических проявлений; отсутствие признаков метаболического синдрома; отсутствие в анамнезе эпизодов назначения и приема антибиотиков в течение последних 6 мес; отказ от приема наркотических и психотропных средств, ядовитых и сильнодействующих веществ, гормональных препаратов в течение последних 6 мес; отказ от употребления алкоголя, табакокурения в течение минимум 3 нед; отсутствие процедуры татуирования, татуажа, пирсинга и пр. в течение последних 6 мес; оценка психического статуса; изучение сведений о диете, привычках питания, физической активности.
После анкетирования потенциальные доноры проходили лабораторное обследование (оценка состояния здоровья добровольца и лабораторная диагностика биологического материала):
- посев кала на микрофлору – выявление патогенной микрофлоры, оценка качественного и количественного состава «полезной» микрофлоры;
- копрограмма;
- анализ кала на скрытую кровь;
- анализ на простейших и яйца гельминтов (микроскопия).
- общий анализ крови с лейкоцитарной формулой;
- биохимический анализ крови (оценивали АЛТ, АСТ, щелочную фосфатазу, амилазу общую, фракции билирубина, уровень глюкозы, мочевину, креатинин);
- анализ на наличие вирусов – ВИЧ, гепатит В и С;
- анализ на наличие возбудителя сифилиса;
- анализ мочи общий;
- анализ кала методом полимеразно-цепной реакции на острые кишечные инфекции, токсины А и В Clostridioides difficile, наличие генов резистентности.
Если все результаты анализов соответствовали нормальным значениям, донора приглашали в медицинское учреждение для повторной сдачи кала.
Бактериологический посев кала
Бактериологический посев кала проводили согласно методическим рекомендациям «Бактериологическая диагностика дисбактериоза», утвержденным Министерством здравоохранения СССР 14.04.1977. Кроме того, проведен расширенный анализ определения лактобактерий с использованием плотных дифференциальных питательных сред и карт биохимической идентификации микробиологического анализатора VITEK® 2 Compact (bioMérieux, Франция).
Статистический анализ
Накопление, корректировку и систематизацию исходной информации выполняли в электронных таблицах Microsoft Office Excel 2020 (разработчик – компания Microsoft, США). Статистическую обработку результатов осуществляли с помощью программ Statistica v. 10 (StatSoft, Россия). Значимость различий оценивали по критерию χ2 Пирсона с поправкой Йейтса. Значимость различий показателей оценивали по критерию Мак-Немара. Различие считали статистически значимым при значениях p<0,05.
Результаты и обсуждение
В ходе анкетирования из 73 здоровых добровольцев первичный отбор не прошли 34 (46,5%) участника исследования: ИМТ не соответствовал норме – 3 (4,1%) человека, возраст старше 55 лет – 4 (5,5%) человека, получали антибактериальную терапию в течение последних 6 мес до участия в исследовании – 11 (15%) человек, наличие аутоиммунных заболеваний – 2 (2,7%) человека, проявление аллергических реакций в анамнезе – 3 человека (4,1%). Кроме того, у 11 (15%) человек в биоматериале (кал) выявлены гены резистентности к антибактериальным препаратам: ген mef, отвечающий за устойчивость Streptococcus spp. к макролидам, и ген ermb, отвечающий за устойчивость Streptococcus spp. и Staphylococcus spp к макролидам, линкозамидам, стрептограминам. Данные участники также не были включены в текущее исследование. Однако ранее нами было показано, что гены резистентности mef и ermB встречаются повсеместно не только у взрослого населения, но и у детей грудного возраста, что может позволить включать данных участников в качестве потенциальных доноров фекальной микробиоты [17]. При этом, наши результаты согласуются с мировыми данными [18].Согласно результатам анкетирования для дальнейшего исследования и проведения лабораторных анализов было включено 39 потенциальных здоровых доноров мужского и женского пола от 22 до 49 лет. Стоит отметить, что возраст здоровых добровольцев фекальной микробиоты может иметь значение: с одной стороны, должен наступить возраст, когда можно подписать добровольное информированное согласие, этот возраст в России начинается с 18 лет; с другой – нужно учитывать увеличение числа хронических заболеваний у лиц старше 40 лет. Дополнительно могут быть учтены пол, этническая принадлежность донора, наличие или отсутствие приверженности определенному типу питания.
Лабораторное обследование является неотъемлемой частью всего процесса отбора доноров для исключения рисков и возможности передачи инфекционных патогенов, а также микроорганизмов с лекарственной устойчивостью. В ходе работы бактериологический анализ кала был проведен всем 39 участникам исследования, копрограмма – 37 участникам, общий и биохимический анализы крови – 36 участникам, общий анализ мочи – 37 участникам. Полный спектр анализов проведен не всем 39 участникам исследования по причине несоответствия результатов бактериологического анализа (который является обязательным для всех доноров ТФМ) нормам, а также отказ самих участников от проведения дальнейших лабораторных исследований.
Бактериологический анализ
Оценка качественного и количественного бактериологического состава образцов кала является ключевым критерием отбора добровольцев, биоматериал которых может быть использован для ТФМ (если все другие показатели лабораторного исследования соответствуют норме). В ходе работы проведена предварительная оценка образцов кала потенциально здоровых добровольцев (n=39). Результаты бактериологического посева в соответствии с отраслевым стандартом 91500.11.0004-2003 «Протокол ведения больных. Дисбактериоз кишечника», утвержденным приказом № 231 Минздрава России от 09.06.2003, представлены в табл. 1.
Таблица 1. Бактериологическое исследование образцов кала потенциально здоровых доноров
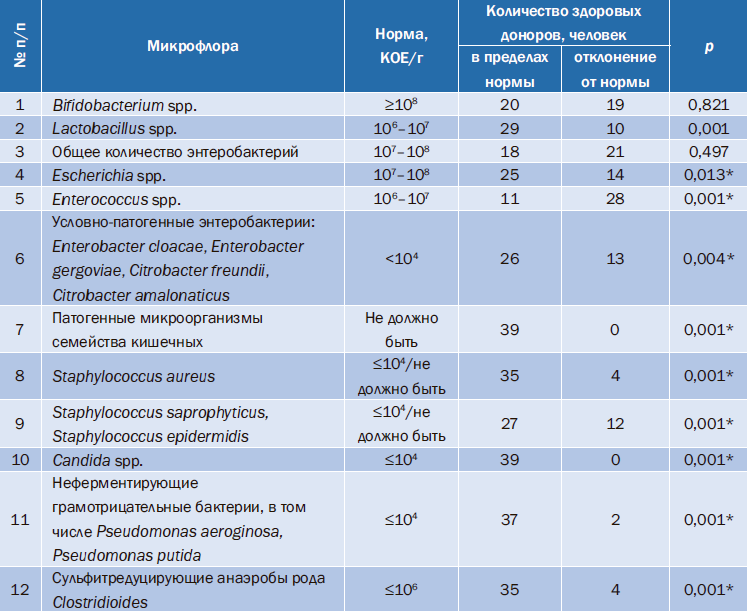
Здесь и в табл. 2: * – достоверность различий при p<0,05.
Из данных, представленных в табл. 1, следует, что у исследуемых добровольцев содержание видов облигатной микрофлоры, таких как Bifidobacterium, Lactobacillus, Escherichia находится в норме у 51,3; 74,4 и 64,1% соответственно, Enterococcus – у 28,2%. Условно-патогенные бактерии факультативной микрофлоры выявлены у 69,2% участников и представлены видами Enterobacter cloacae, Staphylococcus aureus, Citrobacter freundii, Citrobacter amalonaticus, Pseudomonas aeruginosa, Pseudomonas putida, Enterobacter gergoviae.
Таким образом, анализ бактериологического посева показал, что результаты соответствуют нормам по всем показателям только у 10,2% потенциально здоровых доноров, что составляет 4 человека из 39 обследованных.Бактериологическое разнообразие фекальной микробиоты, ее качественный и количественный состав, наличие определенного бактериального состава фекальной микробиоты ассоциировано с успешностью проведения ТФМ.
Так, в исследовании, представленном в 2021 г. J. He с соавт., оптимальный бактериальный состав определялся по преобладанию Bacteroidetes по сравнению с Firmicutes, низким уровнем Fusobacterium и Ruminococcus gnavus, высоким содержанием Akkermansia muciniphila, неклассифицированных Ruminococcaceae, Ruminococcus ssp. и бифидобактерий [19]. Высокое разнообразие фекальной микробиоты ассоциировано с описанием нормальной фекальной микробиоты и микробиологического здоровья кишечника [20].
Микробиологические методы исследования кала, определение качественного и количественного состава облигатных, условно-патогенных и патогенных микроорганизмов наиболее информативны в диагностике соотношения нормальной фекальной микробиоты, позволяют определять наличие живых микроорганизмов кишечника. Дополнительное исследование на лактобактерии как одного из основных видов облигатной микрофлоры кишечника является преимуществом при оценке разнообразия фекальной микробиоты, которую можно называть здоровой. Современные технологии секвенирования 16S-рибосомальной РНК и полногеномного секвенирования дают возможность получить подробную информацию о микробном пейзаже и метаболической активности микробиоты. В проведенном исследовании секвенирование 16S-рибосомальной РНК кала проведено 2 здоровым донорам для верификации отсутствия потенциально патогенной некультивируемой микрофлоры (данные не опубликованы).
Копрограмма
Для оценки физических и химических свойств каловых масс, а также исключения нарушения тех или иных функций пищеварительного тракта 37 потенциальным донорам ТФМ был проведен общий анализ кала. Отклонения по результатам общего анализа кала, включая анализ на скрытую кровь, представлены в табл. 2.
Таблица 2. Копрологическое исследование образцов кала потенциально здоровых доноров
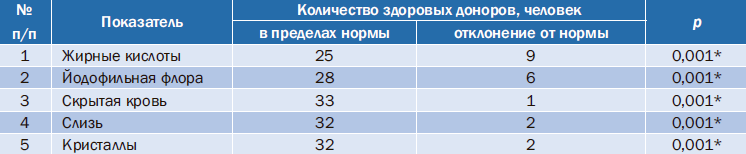
Копрограмма соответствовала норме у 22 участников исследования, что составило 59,5% потенциально здоровых доноров. У одного донора при проведении процедуры скрининга отклонения не выявлены, но при копрологическом исследовании кала на скрытую кровь выявлен положительный результат, что может являться маркером ВЗК и скрытого кровотечения на фоне эрозивно-язвенных поражений слизистой кишечника, колоректального рака. Больше всего отмечаются отклонения от нормы по жирным кислотам и йодофильной флоре, что может свидетельствовать о нарушении процессов пищеварения в ЖКТ, связанных с недостаточной внешнесекреторной функцией поджелудочной железы и употреблением в пищу избыточного количества углеводов.
Общий и биохимический анализ кровиДля оценки состояния здоровья в ходе исследования общий и биохимический анализы крови были проведены 36 потенциальным донорам ТФМ. Отклонения от нормальных показателей крови были выявлены у 9 (25%) участников исследования, в том числе по результатам общего клинического анализа крови отклонения у 7 (19,4%) участников исследования были выявлены в лейкоцитарной формуле (у этих доноров нельзя исключить наличие системных заболеваний, аллергии, поражение органов эндокринной системы, воспалительные процессы). По результатам биохимического анализа отклонения отмечались всего у 2 (5,5%) участников исследования, а именно повышение уровней общего билирубина и АЛТ, что может свидетельствовать о не выявленном при скрининге поражении печени или миокарда.
Таким образом, в ходе представленного исследования по подбору доноров фекальной микробиоты проведен многопараметрический анализ состояния здоровья добровольцев, включающий расширенную оценку качественного и количественного микробного состава кала. Согласно результатам исследования, подбор здорового донора, который отвечает всем критериям отбора, – процесс трудоемкий, и материал (кал), пригодный для ТФМ, встречается редко. Многие бессимптомные добровольцы не прошли скрининг, поскольку у них были выявлены отклонения анализов от нормы. Из всех 39 участников, которые были включены в исследование, только 4 соответствовали критериям отбора доноров фекальной микробиоты, что составило 1,6%. Такой низкий процент соответствия критериям отбора доноров фекальной микробиоты совпадает с данными литературы подобных исследований.
Так, крупнейший банк кала (OpenBiome, Кембридж, Массачусетс) в 2021 г. сообщил, что только 3% потенциальных кандидатов успешно прошли скрининг, в исследованиях S. Paramsothy в 2015 г. по подбору доноров фекальной микробиоты также отмечается, что только 6–10% прошедших скрининг доноров в конечном итоге были признаны подходящими [21], в работах S. Porcari 2023 г. приемлемы 2–20% потенциальных кандидатов [16].
Заключение
Скрининговые программы подбора донора для ТФМ отражают состояние здоровья населения, которое неразрывно связано с его образом жизни. За последнее столетие образ жизни претерпел существенные изменения, что привело к изменению микробиоты, находящейся в динамичном взаимодействии с ЖКТ хозяина, а это делает ее легко изменяемой многими эндогенными и экзогенными факторами.В результате проведенного нами исследования, несмотря на небольшую выборку участников из 73 человек, считающих себя здоровыми, по результатам анализов только 4 из них соответствуют всем критериям подбора донора. Остальные участники исследования имеют те или иные отклонения, которые могут являться биомаркерами наличия скрытых проблем состояния здоровья здорового добровольца.
Таким образом, при проведении процедуры поиска и подбора здоровых доноров фекальной микробиоты невольно осуществляются профилактические проверки здоровья населения. Тщательный, строгий скрининг здоровых добровольцев фекальной микробиоты поможет раннему выявлению заболеваний и их своевременной профилактике, будет способствовать внедрению инноваций в программах чекапов в области практического здравоохранения и инструментах скрининга при проведении клинических исследований, развивать концепцию предиктивной, превентивной, персонализированной медицины будущего.
Обеспечение возможности доступа к необходимым образцам фекальной микробиоты, полученным от здоровых добровольцев, медицинским организациям, исследовательским центрам, фармацевтическим компаниям является ключевым стимулом развития биобанка фекальной микробиоты.
СВЕДЕНИЯ ОБ АВТОРАХ
Господарик Алина Владимировна (Alina V. Gospodaryk) – кандидат биологических наук, научный сотрудник лаборатории молекулярной медицины ЦММиД, ФГБУ ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России, Москва, Российская Федерация
https://orcid.org/0009-0003-7870-1106
Прохорова Наталья Дмитриевна (Natalya D. Prokhorova) – младший научный сотрудник лаборатории молекулярной медицины ЦММиД, ФГБУ ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России, Москва, Российская Федерация
https://orcid.org/0000-0001-6485-1056
Беспятых Юлия Андреевна (Julia А. Bespyatykh) – кандидат биологических наук, руководитель ЦММиД, ФГБУ ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России; доцент кафедры экспертизы в допинг- и наркоконтроле РХТУ им. Д.И. Менделеева; магистр направления «Общественное здравоохранение», ФГБУН «Национальный НИИ институт общественного здоровья имени Н.А. Семашко», Москва, Российская Федерация
https://orcid.org/0000-0002-4408-503X
 Высшая школа организации и управления здравоохранением
Высшая школа организации и управления здравоохранением